|
Chimica Generale ed Inorganica
Corsi di Laurea triennale
________________
Un qualunque oggetto è fatto di materia. La materia è
costituita da piccole particelle, al limite indivisibili (atomI: meno di
90 tipi di atomi sono rintracciabili sulla crosta terrestre). Tutti i possibili oggetti materiali sono costituiti
dalla combinazione di un gran numero di atomi uguali o diversi
La CHIMICA è la scienza che studia la composizione,
la struttura e le proprietà delle varie
sostanze naturali o sintetiche;
indaga sul modo con cui esse si trasformano (reazioni: sintesi, ossidazioni,
riduzioni etc.) e pone particolare attenzione sulle relazioni quantitative che
intervengono in tali trasformazioni (concentrazione di soluzioni, rapporti stechiometrici
etc.).
La CHIMICA è una scienza SPERIMENTALE
Ipotizza MODELLI teorici (atomo, legame, molecola etc.) allo scopo
di interpretare e razionalizzare le proprietà e le trasformazioni
della materia. I modelli sono ritenuti validi finchè non si evidenziano
gravi contraddizioni. Quelli proposti finora hanno permesso di sintetizzare
nuove sostanze chimiche e materiali dotati di speciali proprietà chimiche fisiche
e chimico-fisiche.
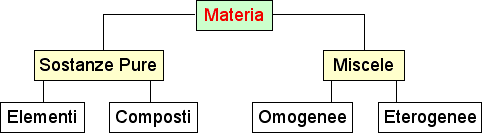
ELEMENTI E COMPOSTI
Gli elementi o sostenze elementari hanno atomi
tutti uguali; i composti hanno due o più tipi
di atomi di elementi diversi.
Gli elementi possono esistere come molecole monoatomiche, come molecole bi-
o pluri-atomche oppure ancora sotto forma di strutture solide
ordinate con atomi tutti uguali.
I composti possono esistere sotto forma di singole molecole (ciascuna molecola
contiene gli atomi dei diversi elementi tipici del composto), oppure sotto forma
di strutture solide complesse e ordinate caratterizzate da un rapporto numerico
ben preciso dei tipi di atomi dei diversi elementi che caratterizzano la formula
del composto stesso.
Mentre sono parecchie milioni le sostanze pure conosciute, quelle elementari
o elementi sono appena un centinaio. Ecco un esempio di (a) un elemento,
(b) un composto e (c) una miscela:
|
a) gas idrogeno
--> molecole (H2) costituite da due atomi uguali
H
|

|
b) Acqua -->
molecole (H2O) costituite da atomi diversi (due H e uno O)
|

|
c) Soluzione (es.
Acqua + Zucchero in miscela omogenea)
|
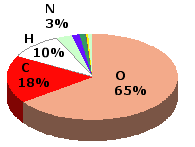
ABBONDANZA DEGLI ELEMENTI
Contenuto percentuale in peso medio degli elementi nel corpo umano:
 |
| |
Elemento |
|
% in peso |
| |
O |
|
64.6 |
| |
C |
|
18 |
| |
H |
|
10 |
| |
N |
|
3.1 |
| |
Ca |
|
1.9 |
| |
P |
|
1.1 |
| |
Cl |
|
0.4 |
| |
K |
|
0.35 |
| |
S |
|
0.25 |
| |
Na |
|
0.11 |
| |
Mg |
|
0.05 |
| |
Cu, Zn, Se, Mo, F, I, Mn, Co, Fe. |
|
0.70 |
| |
Li, Sr, Al, Si, Pb, V, As, Br |
|
tracce |
|
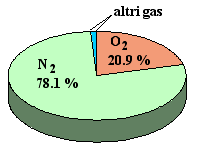
Contenuto percentuale in volume (frazione molare) degli elementi e di altre sostenza nell'aria secca a livello del mare:
 |
| |
Elemento o composto |
|
% in volume |
| |
N2 |
|
78.1 |
| |
O2 |
|
20.9 |
| |
Ar |
|
0.934 |
| |
CO2 |
|
0.035 |
| |
Ne |
|
0.0001818 |
| |
He |
|
0.000524 |
| |
CH4 |
|
0.000217 |
| |
Kr |
|
0.000114 |
| |
H2 |
|
0.000031 |
| |
N2O |
|
0.000031 |
| |
Xe |
|
0.0000087 |
|
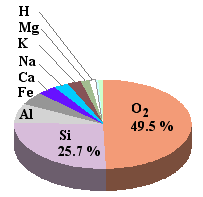
Contenuto percentuale in peso medio degli elementi nella Crosta Terrestre:
 |
| |
Elemento |
|
% in peso |
| |
O |
|
49.5 |
| |
Si |
|
25.7 |
| |
Al |
|
7.4 |
| |
Fe |
|
4.7 |
| |
Ca |
|
3.4 |
| |
Na |
|
2.6 |
| |
K |
|
2.4 |
| |
Mg |
|
1.9 |
| |
H |
|
0.9 |
| |
Ti |
|
0.6 |
| |
Altri (Carbonio 0.09%) |
|
0.9 |
|
|